Hablar de la pérdida de memoria es uno de los temas más complicados por sus amplios factores y espectros. Dentro de las posibles causas encontramos diversas patologías, así como distintos daños a nivel cerebral. De igual manera, partimos del hecho de que muchos de los pacientes con problemas de memoria empatan con múltiples diagnósticos como amnesia, demencia, alzhéimer y deterioro cognitivo, entre otras condiciones de neurodegeneración. Durante el desarrollo de este tema podremos ir respondiendo algunas preguntas sobre la pérdida de memoria por péptido beta-amiloide.
¿Qué es un péptido?
En primer lugar, empecemos explicando qué son los péptidos. Los péptidos son un conjunto reducido de aminoácidos. Sustancias químicas que constituyen el componente básico de las proteínas. De la misma manera, forman parte de la estructura de las membranas celulares. Es decir, son constituyentes esenciales de las células vivas.
Entonces, ¿qué es el péptido beta-amiloide?
En el ámbito científico y biomédico se busca el origen de muchos de los patógenos del cuerpo humano. Uno de estos patógenos es el péptido beta-amiloide (amyloid beta, Aβ, en inglés). Este pertenece a un conjunto de genes y moléculas que regulan la transmisión sináptica en el hipocampo y, a su vez, depende de la actividad neuronal en el sistema nervioso central (SNC).
El péptido se ha considerado en las últimas dos décadas uno de los principales orígenes de la neurodegeneración de la memoria. Un aspecto que se ha observado en diversos estudios experimentales donde se encontraron relaciones a nivel clínico en pacientes con diagnóstico de demencias, como la enfermedad de Alzheimer (EA). Veamos un poco más sobre la relación entre la pérdida de memoria por péptido beta-amiloide.
¿Cómo se conforma?: Papel de la neurodegeneración
En primer lugar, entendemos la neurodegeneración como un principio genético que se ve afectado debido a una alteración molecular. En consecuencia, se van creando placas β-amiloide que son partículas de proteínas deformadas. Estas propician el procesamiento de una sola proteína transmembrana, la proteína precursora amiloidea (APP). La APP es una proteína que se conoce, comúnmente, por sus mecanismos responsables de la EA (Scheuner et al., 1996).
¿Cuál sería el rol del péptido beta-amiloide en el SNC?
Hemos revisado la compleja red genética y molecular asociada a la degeneración neurológica. En la actualidad, hablar de una función específica en la neurodegeneración del péptido beta-amiloide referente a la memoria desata diversas controversias debido al papel que desempeña la fibrilación del péptido. Lo que esto significa es que tendría múltiples afecciones como temblores a nivel motriz o deterioros celulares tanto de manera extracelular como intracelularmente, afectando a otras estructuras del cerebro (Breydo et al., 2016).
Múltiples efectos
Adicionalmente, las fibrilaciones afectan a un gran número de neuronas en áreas específicas del cerebro. Es decir, muchas veces este péptido suele llegar a ser tóxico para un gran número de neuronas. Además, puede causar la formación de poros, lo que da lugar a la fuga de iones (moléculas), alteración del equilibrio del calcio celular y pérdida del potencial electroquímico de membrana en cada una de las neuronas afectadas. En consecuencia, esto irá causando la muerte neuronal (apoptosis) y fallos en la comunicación entre neuronas.

Eventualmente, estos péptidos se combinan con una proteína denominada TAU que se caracteriza, principalmente, por su capacidad de autoreplicarse, generando hiperfosforilación. Lo que significa que existe una alteración que degrada las enzimas que se encargan de regular y favorecer las reacciones químicas existentes en las neuronas.
Así pues, la hiperfosforilación produce un cúmulo anormal de proteínas conocidas como ovillos neurofibrilares. Estos últimos conforman diversas inflamaciones en la neurona que impiden la comunicación neuronal y el intercambio de información a diversas áreas cerebrales. En especial, a ciertas zonas de la memoria.
Implicación de los péptidos beta-amiloide en la neurodegeneración
Muñoz (2001) precisa cuatro estudios de laboratorio demostrando cómo afecta el péptido beta-amiloide en la neurodegeneración. Algunos de ellos son los siguientes:
- Estudios in vitro: Se han podido reproducir procesos que son parecidos a los observados en tejidos postmortem de pacientes con EA.
- Estudios histopatológicos: Este tipo de estudios ha demostrado una fuerte correlación entre la demencia y la presencia de placas seniles (depósitos de péptidos beta-amiloide) en la corteza entorrinal, una de las áreas cerebrales más afectadas en la demencia tipo Alzheimer.
- Casos de aparición temprana de demencia tipo EA: Se han registrado mutaciones que afectan directamente a una secuencia aminoácida o al procesamiento y traducción del péptido beta-amiloide.
- Los individuos con trisomía en el cromosoma 21: Especialistas en psicogeriatría han identificado que este cromosoma es el sitio donde se codifican diversas moléculas para el péptido desarrollando, de esta manera, demencia en edades adultas con una gran abundancia de placas seniles cerebrales.
Pérdida de memoria por péptido beta-amiloide
Se ha logrado detectar que el exceso de péptidos beta amiloide es extremadamente tóxico y nocivo para todo el sistema neuronal. Especialmente, cuando se encuentran focalizados en diferentes áreas específicas del hipocampo. En varios experimentos con modelos de ratón afectados con cepas de dicho péptido, se ha reportado cómo este logra ir generando pérdida de memoria, deteriorando la memoria a largo plazo y el posible desarrollo de depresión a largo plazo.
Esto se ha logrado mediante observación de pacientes que padecen depresión crónica, problemas cognitivos severos, alzhéimer y demencia. De igual modo, se ha observado que los ratones afectados han logrado desarrollar un gran número de placas beta-amiloide en sus células nerviosas.
En consecuencia, la función electrofisiológica se vio alterada, reflejada principalmente, en hiperexcitabilidad y actividad epileptiforme presentando déficits en el rendimiento del aprendizaje y la memoria. Cada vez hay más datos que sugieren que las alteraciones de la red cerebral son debidas a la segregación de componentes como TAU, Aβ y APP, las cuales podrían explicar la patogénesis temprana en diversos problemas de memoria y cognición (Mondragón-Rodríguez et al., 2018).
Alteraciones funcionales de memoria en el hipocampo
Comúnmente, las alteraciones de la memoria por estas placas son más evidentes en la zona del lóbulo temporal donde se ubica el hipocampo, lo cual afecta el procesamiento de información a corto plazo. Sin embargo, este problema no solo ocurre en la memoria, sino en otras funciones cognitivas debido a las conexiones de dicho lóbulo con diversas áreas cerebrales.
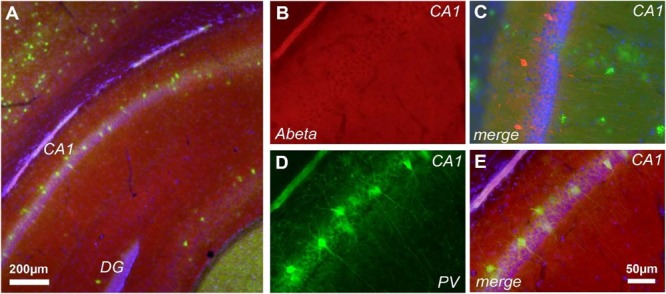
Algunas de las conexiones ocurren de manera directa con el lóbulo frontal y el área anterior a la corteza motora, encargadas de la velocidad psicomotora y la función ejecutiva. Cuando hay déficits en la conexión entre estas regiones con el lóbulo temporal, se van a ver afectadas funciones como la toma de decisiones y el juicio. Asimismo, en las áreas temporofrontales se encuentra la fluidez verbal y la memoria.
Con respecto a las áreas parietooccipitales, toman protagonismo las tareas de función psicomotora compleja. Estas zonas también generan conexiones entre los ganglios basales y el hipocampo para el registro de uno o más caracteres involucrados en la motricidad y la memoria (Martínez y Villagómez, 2019).
Conclusión
A lo largo de esta nota hemos podido observar cómo muchas de las alteraciones de memoria pueden ser causadas por factores orgánicos. Uno de ellos produce pérdida de memoria por péptido beta-amiloide. Generalmente, no se involucran características de lesiones estructurales que pueden ser diagnosticadas de primera instancia, de manera que se vuelve relevante un trabajo multidisciplinario.
Esto implica una atención temprana desde las primeras evaluaciones médicas, neuropsicológicas, neurológicas y de laboratorio. Así pues, la prevención y el tratamiento en las fases iniciales de la pérdida de memoria y neurodegeneración serán más efectivos. Para aprender más sobre las bases neuropsicológicas de esta función cognitiva y cómo evaluarla, te invitamos a nuestro curso sobre memoria.
Referencias bibliográficas
- Breydo, L., Kurouski, D., Rasool, S., Milton, S., Wu, J. W., Uversky, V. N., Lednev, I. K. y Glabe, C. G. (2016). Diferencias estructurales entre los oligómeros beta amiloide. Comunicaciones de investigación bioquímica y biofísica, 477(4), 700-705. https://doi.org/10.1016/j.bbrc.2016.06.122
- Martínez, D. y Villagómez, V. (2019). La diabetes mellitus tipo II asociada a la pérdida de memoria. UNAM, 25-27.
- Mondragón-Rodríguez, S., Gu, N., Manseau, F. y Williams, S. (2018). Alzheimer’s Transgenic Model Is Characterized by Very Early Brain Network Alterations and β-CTF Fragment Accumulation: Reversal by β-Secretase Inhibition. Frontiers in cellular neuroscience, 12(121) 1-17. https://doi.org/10.3389/fncel.2018.00121
- Muñoz López, F. J. (2001). El péptido β-amiloide: mecanismos de neurotoxicidad. neuroprotección por antioxidantes y estrógenos. Revista Española de Geriatría y Gerontología, 36(2), 109-116. https://doi.org/10.1016/S0211-139X(01)74694-X
- Saitoh, T., Sundsmo, M., Roch, J. M., Kimura, N., Cole, G., Schubert, D., Oltersdorf, T. y Schenk, D. B. (1989). Secreted form of amyloid beta protein precursor is involved in the growth regulation of fibroblasts. Cell, 58(4), 615-622. https://doi.org/10.1016/0092-8674(89)90096-2
- Scheuner, D., Eckman, C., Jensen, M., Song, X., Citron, M., Suzuki, N., Bird, T. D., Hardy, J., Hutton, M., Kukull, W., Larson, E., Levy-Lahad, E., Viitanen, M., Peskind, E., Poorkaj, P., Schellenberg, G., Tanzi, R., Wasco, W., Lannfelt, L., Selkoe, D. y Younkin, S. (1996). Secreted amyloid beta-protein similar to that in the senile plaques of Alzheimer’s disease is increased in vivo by the presenilin 1 and 2 and APP mutations linked to familial Alzheimer’s disease. Nature medicine, 2(8), 864-870. https://doi.org/10.1038/nm0896-864